Koniec monopolu leków biologicznych w UE? Krajowi Producenci Leków alarmują: Akt o Biotechnologii może uderzyć w pacjentów
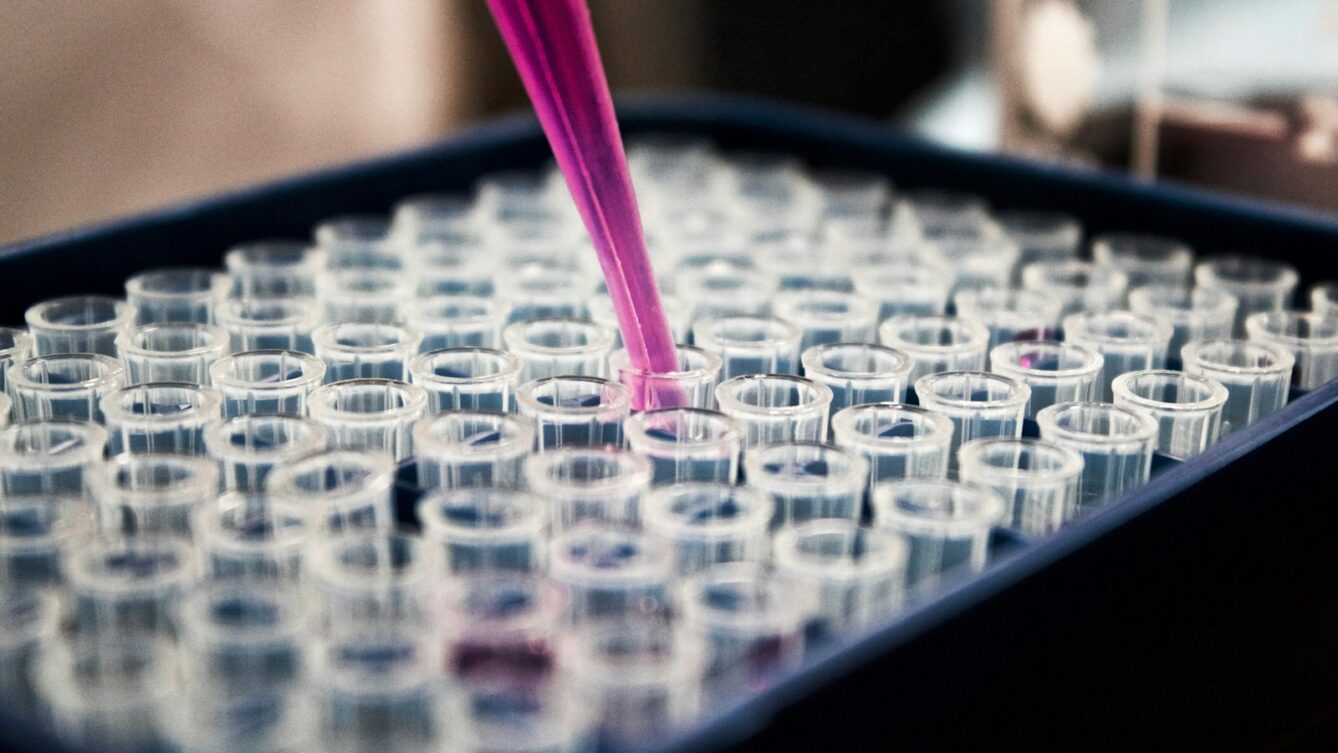
W Unii Europejskiej ważą się losy Aktu o Biotechnologii (Biotech Act). Choć dokument ma wspierać innowacje, polscy i europejscy producenci leków ostrzegają: proponowane zmiany w ochronie patentowej mogą zablokować rozwój tańszych terapii. To może kosztować systemy opieki zdrowotnej miliardy euro.
W tym roku mija 20 lat, odkąd na europejskim rynku pojawiła się pierwsza konkurencja dla leków biologicznych – efekt wygaśnięcia monopolu somatropiny. Od tego czasu leki biologiczne równoważne (biosymilary) stały się fundamentem nowoczesnej medycyny. Dodatkowo drastycznie zwiększają dostęp pacjentów do zaawansowanych terapii. Podczas konferencji BIOS26 w Amsterdamie eksperci podkreślali, że sektor ten jest strategicznym filarem europejskiej bioekonomii. Jednak jego dalszy rozwój zależy od ostatecznego kształtu unijnych przepisów. Te regulacje mogą albo przyspieszyć budowę suwerenności lekowej, albo opóźnić wejście na rynek tańszych odpowiedników.
Miliardowe oszczędności zagrożone
Od 2006 r. leki biologiczne wprowadzane na rynek jako konkurencja do kończących monopol produktów wygenerowały 75 mld euro oszczędności dla systemów opieki zdrowotnej w UE i stanowiły 40%rejestrowanych w 2025 r. w Europejskiej Agencji Leków EMA produktów.
Nowo wynaleziony lek biologicznych jest chroniony patentem przez 20 lat i przez kolejne 5 lat przez Dodatkowe Prawo Ochronne (SPC– Supplementary Protection Certificate). Po wygaśnięciu monopolu wielu wytwórców zaczyna go produkować, a konkurencja na rynku obniża cenę. Dzięki temu więcej chorych może zostać objętych leczeniem.
Mimo to, projekt Aktu o biotechnologii proponuje wydłużenie Dodatkowego Prawa Ochronnego (SPC) o kolejne 12 miesięcy. Zdaniem branży, to krok w złym kierunku.
Dlatego ważne jest, aby powstające prawo wspierało rozwój sektora leków biologicznych równoważnych konkurujących ceną. Tymczasem w przygotowanym przez Komisję Europejską projekcie Aktu o biotechnologii proponuje się wydłużenie monopolu leku – ostrzega Krzysztof Kopeć, prezes Krajowych Producentów Leków.
Kosztowny monopol: 7,7 mld euro za trzy leki
Przedłużenie ochrony o rok może wydawać się krótkim okresem, ale w skali całej Unii oznacza gigantyczne wydatki. Wyliczono, że opóźnienie konkurencji dla zaledwie trzech kluczowych cząsteczek onkologicznych (Keytruda®, Darzalex®, Opdivo®) to koszt rzędu 7,7 mld euro rocznie. Kwota ta stanowi ponad połowę oszczędności, jakie UE czerpie obecnie z całej konkurencji biosymilarów.
To będzie blokować rozwój sektora w Europie. SPC i tak już teraz przedłuża monopol nawet o 5 lat, a UE ma jeden z najdłuższych okresów takiej ochrony na świecie– wskazuje Grzegorz Rychwalski, wiceprezes Krajowych Producentów Leków.
Ustawodawcy UE mają wyjątkową szansę na stworzenie przewagi konkurencyjnej w tym sektorze poprzez zachęcanie do inwestycji w produkcję dzięki dedykowanym funduszom i przyjaznym przepisom dotyczącym zwolnień z SPC. Nie powinniśmy tej szansy marnować – dodaje Krzysztof Kopeć.
Adrian van den Hoven z europejskiej organizacji zrzeszającej producentów leków Medicines for Europe, której Krajowi Producenci Leków są członkiem, ostrzega, że rozszerzanie SPC będzie kosztować systemy opieki zdrowotnej miliardy euro rocznie, na które przecież ich nie stać.
Polska farmacja świetnie tłucze suplementy i generyki, ale nie produkuje leków krytycznych. Alarmujący raport INNOWO
Walka o suwerenność lekową i „Dolinę Śmierci”
Obecnie około 46% biosymilarów stosowanych w Europie jest produkowanych na naszym kontynencie, ale aż 54% pochodzi spoza UE. Eksperci wskazują, że Europa zmaga się z tzw. „doliną śmierci” – trudnością w skalowaniu innowacji z laboratoriów do fabryk. Choć KE zapowiada wsparcie, brakuje jasnych kryteriów dla producentów leków równoważnych.
Ustawodawcy UE mają wyjątkową szansę na stworzenie przewagi konkurencyjnej w tym sektorze poprzez zachęcanie do inwestycji w produkcję dzięki dedykowanym funduszom i przyjaznym przepisom dotyczącym zwolnień z SPC. Nie powinniśmy tej szansy marnować – dodaje Krzysztof Kopeć.
Prezes KPL przypomina również o skali potrzebnego finansowania:
Mamy 20 mld euro w przyszłych ramach finansowych UE i 10 mld w inicjatywie BioTechEU. Jednak bez jasnych zasad dostępności, te środki mogą ominąć sektor leków biologicznych równoważnych. Jeśli chcemy, żeby inwestycje zostawały w Europie, potrzebujemy przewidywalnych zasad i równego dostępu do finansowania. Dziś 46% biosymilarów stosowanych w Europie jest produkowanych w UE, a 54% pochodzi spoza Europy.
Bariery w Polsce i błędy polityki zakupowej
Rozwój leku biologicznego to proces trwający dekadę i kosztujący do 300 mln euro. Tymczasem obecne systemy przetargowe w wielu krajach, w tym w Polsce, skupiają się wyłącznie na najniższej cenie. To zniechęca do budowy lokalnych zdolności produkcyjnych.
Jeden zwycięzca przetargu, presja cenowa oraz brak przewidywalności nie zachęcają do inwestycji – ocenia Grzegorz Rychwalski.
W efekcie mniej niż 30% leków, które stracą wyłączność do 2032 roku, ma dziś rozwijane konkurencyjne odpowiedniki. Branża apeluje o zmianę paradygmatu:
Potrzebujemy modeli z wieloma dostawcami i bardziej zrównoważonej polityki cenowej – podsumowuje Krzysztof Kopeć.
Akt o Biotechnologii ma zostać ostatecznie przyjęty przez Parlament Europejski i Radę prawdopodobnie pod koniec 2026 roku. Do tego czasu organizacje branżowe zapowiadają walkę o przepisy, które realnie wesprą europejską produkcję i bezpieczeństwo pacjentów.
Innowacje czy bezpieczna produkcja? Dlaczego Polska „stoi” generykami
W debacie o suwerenności lekowej często pada pytanie: dlaczego polskie firmy farmaceutyczne skupiają się na lekach generycznych i suplementach, zamiast masowo inwestować we własne, przełomowe cząsteczki? Odpowiedź leży w twardej ekonomii i modelu ryzyka. On determinuje kierunki rozwoju rodzimego przemysłu.
Koszt innowacji vs. możliwości rynku
Opracowanie nowego leku oryginalnego to koszt rzędu 1,5–2,5 mld dolarów oraz dekada badań obarczonych gigantycznym ryzykiem porażki (blisko 90% projektów upada na etapie testów klinicznych). Dla polskich firm, które budowały swoją pozycję na optymalizacji kosztów i dostarczaniu tanich leków, postawienie wszystkiego na jedną innowacyjną kartę jest często barierą nie do przejścia. Zwłaszcza dzieje się tak bez systemowego wsparcia państwa.
Rozwój leku biologicznego równoważnego to 150–300 mln euro i nawet 10 lat pracy
– przypomina Krzysztof Kopeć, prezes Krajowych Producentów Leków. To kwoty, które polskie firmy muszą wyłożyć z własnych środków. Konkurują z globalnymi gigantami dysponującymi budżetami badawczymi wielokrotnie przekraczającymi przychody całego polskiego sektora.
Pułapka najniższej ceny
Kolejną barierą jest model zakupowy polskiego systemu ochrony zdrowia. Przez lata jedynym kryterium w przetargach była najniższa cena, co faworyzowało dostawców z Azji, gdzie koszty produkcji są drastycznie niższe.
Jeden zwycięzca przetargu, presja cenowa oraz brak przewidywalności nie zachęcają do inwestycji
– zauważa Grzegorz Rychwalski. Krajowe firmy, chcąc utrzymać stabilność finansową, wybierają produkcję generyków. Ta produkcja daje przewidywalny zwrot, pozwalający na utrzymanie fabryk i tysięcy miejsc pracy w Polsce.
Krew: Jedyny lek, którego nie wyprodukujemy w laboratorium
Rola Biotech Act: Opóźnienie, które kosztuje
W tym kontekście unijny Biotech Act i proponowane wydłużenie ochrony patentowej (SPC) o 12 miesięcy to problem. Dla polskiej firmy to dodatkowy rok czekania na wejście z tańszym zamiennikiem. W biznesie farmaceutycznym rok zwłoki oznacza nie tylko utracone zyski, ale przede wszystkim brak kapitału. Ten kapitał mógłby zostać przeznaczony na… właśnie na przejście z „tłuczenia generyków” do tworzenia zaawansowanych leków biologicznych.
Jak przełamać ten trend?
Raport INNOWO oraz głosy ekspertów wskazują, że najwięcej zależy od nas samych. Aby polski przemysł mógł inwestować w leki krytyczne i innowacje, potrzebne są:
- Dywersyfikacja dostawców: Rezygnacja z modelu „jeden najtańszy” na rzecz bezpieczeństwa dostaw.
- Premia za lokalną produkcję: Realne wsparcie dla firm, które decydują się na kosztowną syntezę substancji czynnych (API) w Europie.
- Jasne zasady finansowania: Skuteczne wykorzystanie unijnych funduszy (jak BioTechEU). To może zdjąć z barków krajowych firm część ryzyka związanego z badaniami innowacyjnymi.
Bez tych zmian polska farmacja pozostanie sprawną „mieszalnią” i producentem suplementów. Suwerenność lekowa – mimo dużego potencjału naszych inżynierów – pozostanie w sferze planów.
Źródło: PZPPF
Czytaj więcej



